臻和科技助力周彩存教授团队牵头的全国多中心研究成果发表
迄今为止,免疫检查点抑制剂(ICI)已经显著改善了晚期肺鳞状细胞癌(LUSC)的治疗疗效。多项研究表明,免疫检查点抑制剂联合化疗可显著延长晚期肺鳞癌患者的无进展生存期(PFS)和总生存期(OS)。然而这种联合治疗方案的预测性生物标志物在很大程度上仍是未知的。肿瘤突变负荷(Tumor mutation burden, TMB)是ICI单药治疗各种实体肿瘤疗效的候选生物标志物,但相当大比例的患者无法提供足够的组织用于下一代测序(NGS)计算TMB。由于利用外周血循环肿瘤DNA (ctDNA)计算的血液肿瘤突变负荷 (Blood tumor mutation burden, bTMB),具有简便性、无创性,并且能矫正肿瘤异质性或低肿瘤占比带来的抽样偏差,以及实现对早期治疗进行动态监测的优势,从而成为一种更有潜力的方法。
近日,恒瑞医药联合上海市肺科医院周彩存教授团队牵头合作的全国多中心研究成果发表于“Molecular Cancer”(IF:27.401)。文章题为“On-treatment blood TMB as predictors for camrelizumab plus chemotherapy in advanced lung squamous cell carcinoma: biomarker analysis of a phase III trial”。作为唯一参与该研究的肿瘤精准诊断企业,臻和科技承担了该研究的基因测序与相关分析等工作。
主要研究内容
恒瑞医药、上海市肺科医院周彩存教授团队合作开展的CameL-sq研究(NCT03668496)是一项随机、双盲、多中心三期临床试验,以评估卡瑞利珠单抗联合化疗在晚期肺鳞癌一线治疗中的有效性和安全性。研究表明,相比化疗,卡瑞利珠单抗联合化疗作为晚期肺鳞癌患者一线治疗的方案,显著提高了患者的PFS和OS。同时此研究还创新地使用了治疗期bTMB及动态bTMB(∆bTMB=治疗期bTMB-治疗前bTMB)作为检测指标。研究结果表明,bTMB和∆bTMB均可以有效预测晚期肺鳞癌患者卡瑞利珠单抗联合化疗的疗效。
关键结论
治疗期bTMB及其动态∆bTMB可作为晚期LUSC患者卡瑞利珠单抗(Camrelizumab)联合化疗的预测性生物标志物。
研究设计
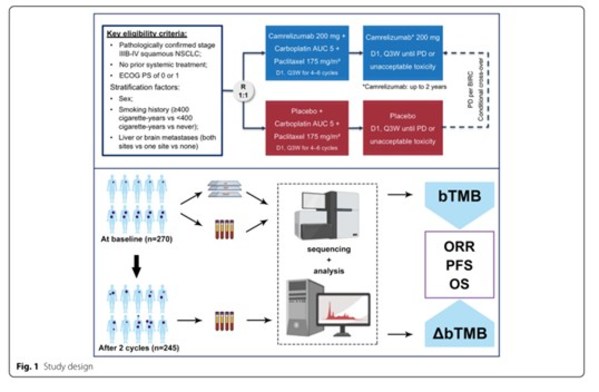
此研究共招募了病理确认为IIIB-IV期,且之前未进行过全身治疗,也无EGFR敏感突变或者ALK相关的基因组变异的389名肺鳞癌患者,并随机分组进行卡瑞利珠单抗联合化疗(n=193)或安慰剂加化疗(n=196)的治疗。其有270名患者收集到基线时的肿瘤组织样本和基线血(卡瑞利珠单抗联合化疗n=134,化疗n=136)样本以及245例治疗期外周血样本,并纳入此生物标志物研究分析,以探讨治疗前tTMB , 治疗前bTMB,治疗期bTMB 和动态∆bTMB对晚期肺鳞癌患者卡瑞利珠单抗联合化疗的疗效预测价值,研究设计如图1所示。
研究结果
1. 治疗期bTMB是预测免疫治疗联合化疗疗效和预后的有效生物标志物
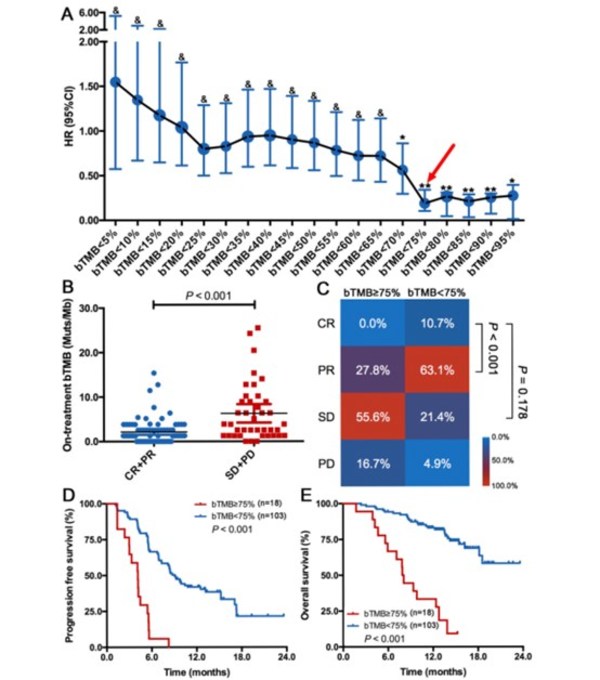
为了更好地体现bTMB预测预后的价值,研究将bTMB值≥75%的组定义为高bTMB组,bTMB值<75%的组定义为低bTMB组(图2A)。在卡瑞利珠单抗联合化疗组中,CR+PR患者的治疗期bTMB显著低于SD+PD患者(P < 0.001,图2B)。同时,治疗期bTMB低的患者,其ORR显著高于治疗期bTMB高的患者(73.8% vs 27.8%, P < 0.001,图2C),其PFS (中位数 9.1 vs 4.1 月; HR = 0.190, P < 0.001; 图2D)和OS (中位数 未达到 vs 8.0 月; HR = 0.144, P < 0.001; 图2E)也显著延长。且经过临床信息/治疗前tTMB和治疗前bTMB的多因素矫正后,治疗期bTMB仍然与PFS(adjusted HR = 0.189; 95%, 0.101–0.358; P < 0.001)和OS(adjusted HR = 0.152; 95% CI, 0.075–0.308; P < 0.001)独立相关。然而在化疗组,治疗期bTMB与ORR和PFS均无相关性。以上结果表明治疗前tTMB和bTMB不能很好地预测卡瑞利珠单抗联合化疗的疗效和预后,而治疗期的bTMB则可以很好地预测卡瑞利珠单抗联合化疗的疗效和预后。
2. 动态bTMB可作为预测免疫治疗联合化疗疗效和预后的补充生物标志物
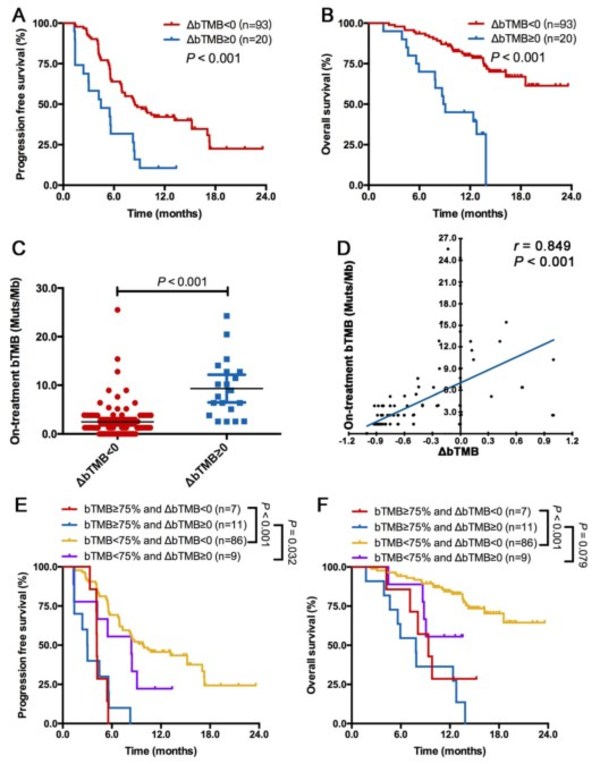
进一步研究表明,动态bTMB(∆bTMB=治疗期bTMB-治疗前bTMB)也可预测免疫治疗联合化疗的疗效和预后。bTMB增加或不变的患者 (∆bTMB ≥0),其PFS (中位数,4.5个月vs 8.5个月;HR= 2.545, p < 0.001;图3A)和OS(中位数,9.0个月vs未达到;HR = 4.199, p = 0.201;图3B)均明显缩短。尽管∆bTMB与治疗期bTMB呈显著相关性(rSpearman= 0.849, P < 0.001,图3D),但将∆bTMB与治疗期bTMB联合进行生存分析时发现它们可以互补地,非重复地预测疗效。具体为,治疗期bTMB低且∆bTMB <0的患者PFS和OS最长,治疗期bTMB低且∆bTMB <0或∆bTMB≥0的患者PFS和OS居中,治疗期bTMB高且∆bTMB≥0的患者PFS和OS最差(P < 0.001;图3E、F)。
3. 治疗期bTMB可从初始放疗SD的患者中鉴定出能长期获益于免疫治疗的患者
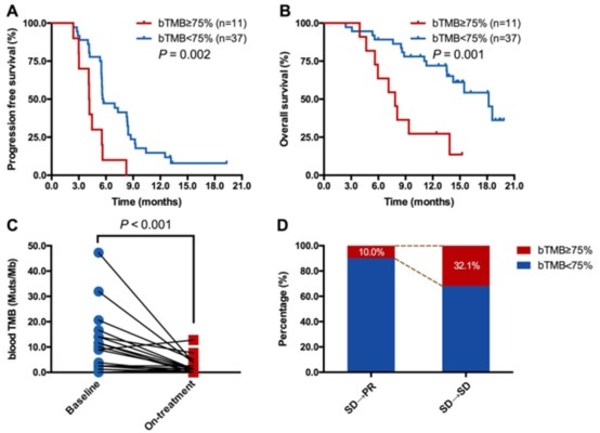
目前,从初始放疗SD患者中区分免疫治疗长期获益的人群仍是一个挑战。考虑到治疗期bTMB和肿瘤负荷之间的相关性,此研究又进一步探索了治疗期bTMB能否区分最初放疗SD但最终获益于免疫治疗的人群。对卡瑞利珠单抗联合化疗组中48例初始放疗SD患者进行分析发现,治疗期bTMB高的患者其PFS(中位数,4.1 vs 5.6个月;HR = 2.861, p = 0.002;图4A)和OS(中位数,7.8 vs 18.2个月;HR = 3.546, p = 0.001;图4B)均显著更低。而对于20例初始放疗SD,但最佳评效为PR的患者,其治疗期bTMB明显低于其对应的基线bTMB (P < 0.001;图4 C),治疗期bTMB≥75%的比例也低于最佳评效为SD的人群(10.0% vs 32.1%;图4 D)。
临床意义
本研究基于血浆肿瘤突变负荷(bTMB)及∆bTMB的分析数据,首次报道了治疗期bTMB与卡瑞利珠单抗联合化疗的ORR/PFS/OS的显著相关性,以及动态∆bTMB对此的补充和非重复性预测效果。此外,治疗期bTMB还能从放疗SD的患者中,鉴定出可在卡瑞利珠单抗联合化疗治疗中长期获益的人群。综上所述,对于晚期肺鳞癌患者,治疗期bTMB可作为预测免疫治疗疗效和预后的有效分子标志物。
研究原标题
On-treatment blood TMB as predictors for camrelizumab plus chemotherapy in advanced lung squamous cell carcinoma:biomarker analysis of a phase III tria .Jiang et al. Molecular Cancer (2022) 21:4;https://doi.org/10.1186/s12943-021-01479-4